Условие задачи:
Через раствор медного купороса пропускают ток, изменяющийся по линейному во времени закону \(I=10-0,02t\) (А). Сколько меди выделится на катоде через 200 с после пропускания такого тока?
Задача №7.3.24 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
\(I=10-0,02t\) А, \(t=200\) с, \(m-?\)
Решение задачи:
 Для нахождения массы меди, выделившейся на катоде, необходимо использовать объединенный закон Фарадея:
Для нахождения массы меди, выделившейся на катоде, необходимо использовать объединенный закон Фарадея:
\[m = \frac{1}{F}\frac{M}{n}It\;\;\;\;(1)\]
Здесь \(F\) — число Фарадея, равное 96600 Кл/моль; \(M\) — молярная масса меди, равная 0,064 кг/моль; \(n\) — валентность меди, равная 2.
Произведение тока \(I\) на время \(t\) равно заряду \(q\), протекшему через электролит, поэтому можем представить формулу (1) в виде:
\[m = \frac{1}{F}\frac{M}{n}q\]
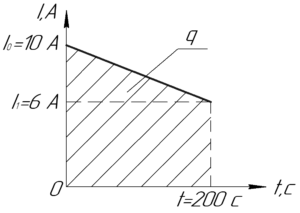
Заряд \(q\) можно найти, если построить график данной в условии линейной функции. Очевидно, что начальный ток \(I_0\) (то есть ток в момент времени \(t=0\) с) равен 10 А, а конечный \(I_1\) (то есть ток в момент времени \(t=200\) с):
\[I_1 = 10 — 0,02 \cdot 200 = 6\;А\]
Если теперь построить график этой линейной функции (а мы это можем сделать, поскольку знаем координат двух точек), то заряд \(q\) равен площади фигуры под графиком функции (смотрите рисунок). Эта фигура является трапецией, поэтому:
\[q = \frac{1}{2}({I_0} + {I_1})t\]
Посчитаем численное значение \(q\):
\[q = \frac{1}{2} \cdot (10 + 6) \cdot 200 = 1600\;Кл\]
В итоге масса \(m\) равна:
\[m = \frac{1}{{96600}} \cdot \frac{{0,064}}{2} \cdot 1600 = 5,3 \cdot {10^{ — 4}}\;кг = 0,53\;г\]
Ответ: 0,53 г.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
7.3.23 Сила тока, характеризующая поток электронов в электронно-лучевой трубке, 400 мкА
7.3.25 Определить массу меди, выделившейся из раствора медного купороса за 100 с, если сила тока
7.3.26 Электрохимический эквивалент меди 3,3×10^(-7) кг/Кл. Сколько меди выделится на электроде