Условие задачи:
Сосуд объемом 5 л разделен перегородкой на две части, заполненные одним газом под давлением 80 и 30 кПа. После удаления перегородки в сосуде установилось давление 70 кПа. Определить, какой объем имела часть сосуда с большим давлением.
Задача №4.2.97 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
\(V=5\) л, \(p_1=80\) кПа, \(p_2=30\) кПа, \(p=70\) кПа, \(V_1-?\)
Решение задачи:
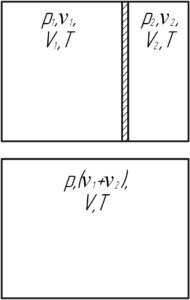 Запишем три раза уравнение Клапейрона-Менделеева: для частей газа по обе стороны от перегородки до её удаления и для всего газа после удаления перегородки. Будем считать, что температура газа всегда оставалась неизменной.
Запишем три раза уравнение Клапейрона-Менделеева: для частей газа по обе стороны от перегородки до её удаления и для всего газа после удаления перегородки. Будем считать, что температура газа всегда оставалась неизменной.
\[\left\{ \begin{gathered}
{p_1}{V_1} = {\nu _1}RT \;\;\;\;(1)\hfill \\
{p_2}{V_2} = {\nu _2}RT \;\;\;\;(2)\hfill \\
pV = \left( {{\nu _1} + {\nu _2}} \right)RT \;\;\;\;(3)\hfill \\
\end{gathered} \right.\]
Сложим уравнения (1) и (2), тогда получим:
\[{p_1}{V_1} + {p_2}{V_2} = \left( {{\nu _1} + {\nu _2}} \right)RT\]
Правые части полученного равенства и уравнения (3) равны, поэтому:
\[{p_1}{V_1} + {p_2}{V_2} = pV\]
Очевидно, что сумма объемов \(V_1\) и \(V_2\) равна объему сосуда \(V\):
\[{V_1} + {V_2} = V\]
\[{V_2} = V — {V_1}\]
Тогда имеем:
\[{p_1}{V_1} + {p_2}\left( {V — {V_1}} \right) = pV\]
Осталось только из этого равенства выразить объем \(V_1\), для чего раскроем скобки в левой части:
\[{p_1}{V_1} + {p_2}V — {p_2}{V_1} = pV\]
\[\left( {{p_1} — {p_2}} \right){V_1} = \left( {p — {p_2}} \right)V\]
\[{V_1} = \frac{{\left( {p — {p_2}} \right)V}}{{{p_1} — {p_2}}}\]
Переведём объем сосуда в систему СИ (из литров в кубические метры):
\[5\;л = 0,005\;м^3\]
Посчитаем ответ:
\[{V_1} = \frac{{\left( {70 \cdot {{10}^3} — 30 \cdot {{10}^3}} \right) \cdot 0,005}}{{80 \cdot {{10}^3} — 30 \cdot {{10}^3}}} = 0,004\;м^3\]
Ответ: 0,004 м3.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
4.2.96 Состояние одного киломоля идеального газа менялось по графику 1-2-3. Определить
4.2.98 При некотором процессе идеального газа связь между давлением и объемом газа pV^3=const
4.2.99 Воздушный шар объемом 1000 м3 наполнен гелием при температуре окружающего воздуха